|
العلاقة بين ذرية العنصر ومجموعته في الجدول الدوري
الاختبار
القبلي / البعدي
1.
|
 |
|
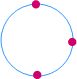
الذرية |
نوعية الأيون |
مجموعة العنصر في الجدول الدوري |
|
ثلاثية |
موجب |
الثالثة
(IA) |
|
|
|
 |
|
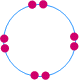
الذرية |
نوعية الأيون |
مجموعة العنصر في الجدول الدوري |
|
صفر |
غير
موجود |
الثامنة
(VIIIA)
أو المجموعة صفر أو الغازات النبيلة |
|
|
|
 |
|
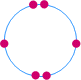
الذرية |
نوعية الأيون |
مجموعة العنصر في الجدول الدوري |
|
ثنائية |
سالب |
السادسة
(VIA) |
|
|
|
 |
|
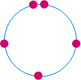
الذرية |
نوعية الأيون |
مجموعة العنصر في الجدول الدوري |
|
ثلاثية |
سالب |
الخامسة
(VA) |
|
|
2.
|
أ- السيليكون في
SiH4
|
ذريته
(4) |
|
ب-
الكربون في
C3H6
|
ذريته (2) |
|
جـ- الحديد في
التفاعل المعطى
|
ذريته (2)
|
|
د- الألومنيوم
في التفاعل المعطى |
ذريته
(3) |
لاحظ في هذا التفاعل أن
ذرتين من الألومنيوم أخذتا محل (6) ذرات من الهيدروجين . إذن ذرة ألومنيوم
واحدة تحل محل ثلاث ذرات من الهيدروجين .
3.
|
رمز
العنصر أو الأيون |
العدد الذري |
عدد
الالكترونات |
توزيع الكترونات العنصر أو الأيون على المستويات |
استخدام إشارة (ü)
لانطباق قاعدة الثمانية وإشارة (û)
لعدم انطباقها |
|
المستوى الأول |
المستوى الثاني |
المستوى الثالث |
|
|
Ne |
10 |
10 |
2 |
8 |
ـــــــ |
ü |
|
S-2 |
16 |
18 |
2 |
8 |
8 |
ü |
|
Mg |
12 |
12 |
2 |
8 |
2 |
û |
|
K+1 |
19 |
18 |
2 |
8 |
8 |
ü |
|
Cl |
17 |
17 |
2 |
8 |
7 |
û |
|

