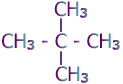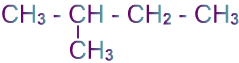|
|||||||||||||||||||||||||||||||||||||||||||
قوى فان دير فال أو قوى لندن :
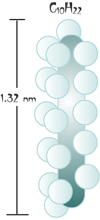
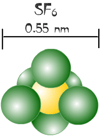
أما الجزيئات التي تعمل فيها قوى فان دير فال وتختلف في
شكلها وحجمها فتعتمد درجة غليانها على هذا الأمر وليس على
كتلتها المولية والأمثلة التالية توضح ذلك :
مثال 2 :
ح) تعرف ثنائيات القطب اللحظية التي تنشأ بين الجزيئات
عديمة القطبية باسم قوى ـــــــ
.
سؤال :
|
|||||||||||||||||||||||||||||||||||||||||||
|
Copyright © 2001 - 2010 SchoolArabia. All rights reserved الحقوق القانونية و حقوق الملكية الفكرية محفوظة للمدرسة العربية |
|||||||||||||||||||||||||||||||||||||||||||