|
التفاعلات
بين الحموض والقواعد
المعايرة
الدرس الأول |
|
عرفت سابقاً، أن
إضافة الحمض إلى القاعدة (أو العكس) ينتج عنه تكوّن الملح، كما
درست أيضاً أن محاليل
الأملاح منها ما هو :
أ- حمضي التأثير (PH
ه<
7)
-
ملح ناتج من حمض قوي وقاعدة ضعيفة.
ب- متعادل التأثير (PH
ه=ه
7) -
ملح ناتج من حمض قوي وقاعدة قوية.
جـ - قلوي التأثير (PHه
> 7)
-
ملح ناتج من حمض قاعدة قوية وحمض ضعيف.
المعايرة :
هي عملية الإضافة التدريجيـة من القاعـدة
إلى الحمض (أو العكس) لمعرفة تركيز مجهول
من الحمض أو القاعدة بوجود
كاشف مناسب.
والآن لنفترض إضافة قاعدة بشكل تدريجي لمحلول حمضي:
1 ـ
بداية يكون المحلول حمضي
PH
له أقل من
7.
2 ـ وعند إضافة قاعدة بشكل تدريجي فهذا يعني
إضافة
- OH
، وبالتالي تزداد قيمة
PH
للمحلول.
3 ـ
وباستمرار إضافة القاعدة للحمض سنصل إلى نقطة يكون فيها:
عـدد مولات الحمض
H3O+
في المحلول
=
عدد مولات القاعدة
- OH
المضافة.
ويطلق
على هذه النقطة (
نقطة التكافؤ )
ه4
ـ
وباستمرار إضافة القاعدة إلى المحلول بعد نقطة التكافؤ سيحدث
ارتفاع في قيمة
PH
للمحلول، ويصبح المحلول قاعدياً.
وبشكل عام، فإن المعايرة تكون بين:
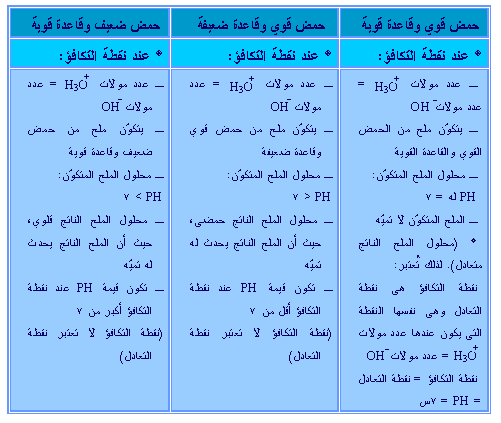
ولتوضيح الجدول السابق، نقول أنه في حالة:
1
ـ
معايرة حمض HCl
مع NaOH:
ـ حيث أن قيمة
PH
عند نقطة التكافؤ=
7 . ولذلك تعتبر نقطة التكافؤ هي
نقطة
التعادل.
ـ الملح الناتج هو
NaCI
، وهو ملح متعادل (لا تميّه).
2
ـ
معايرة حمض HCl
مع NH3:
ـ وتكون قيمة
PH
عند نقطة التكافؤ < 7 .
ـ الملح الناتج هو NH4Cl
، وهو ملح حمضي (يتميّه) (اكتب معادلة التميّه).
3
ـ
معايرة حمض HCN
مع NaOH:
ـ تكون قيمة
PH
عند نقطة التكافؤ > 7 .
ـ الملح الناتج هو
NaCN
، وهو ملح قلوي (يتميه) (اكتب معادلة التميّه).
|
