|
|
||||||||||||||
|
القانون الدوري والجدول الدوري
5.
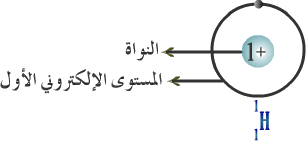
المستويات الإلكترونية ورسم الذرات :
المستوى الأول
(1)
وهو أقربها إلى النواة ،
والمستوى السابع (VII) وهو أبعدها عن
النواة ، ويوجد هذا المستوى في عدد
قليل من العناصر الثقيلة وأولها عنصر
السيزيوم
i 87Cs وما
يليه من عناصر
.
|
||||||||||||||
|
Copyright © 2001 - 2010 SchoolArabia. All rights reserved الحقوق القانونية و حقوق الملكية الفكرية محفوظة للمدرسة العربية |
||||||||||||||

 ).
).