|
الفصل الخامس : الحسابات من
المعادلات الكيميائية (2)
تمهيد :
9. يتفاعل الصوديوم مع الكلور بوجود ضوء الشمس منتجاً كلوريد
الصوديوم حسب المعادلة :
إذا مزج مول واحد من الصوديوم مع كمية زائدة من غاز الكلور ،
فما عدد مولات كلوريد الصوديوم التي يجب أن تنتج ؟ إذا كان
الناتج الحقيقي من كلوريد الصوديوم = 0.9 مول ، فما النسبة
المئوية للناتج ؟؟
تحليل السؤال :
من
الواضح أن كل مول من الصوديوم ينتج مولاً واحداً من كلوريد
الصوديوم ، وبما أن الكلور موجود وبكمية زائدة إذن الناتج
النظري المتوقع من كلوريد الصوديوم تحدده كمية الصوديوم
المتفاعلة . إذن من المتوقع أن تكون كمية كلوريد الصوديوم = 1
مول .
لكن الناتج الحقيقي =
------
مول .
|
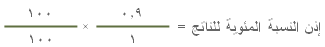
=
------
|
تسمى
النسبة
المئوية للناتج الفعلي مقارنة بالنتائج النظرية باسم
النسبة المئوية للناتج
.
إجابة الأسئلة
|